Entkalken in der Meeresaquaristik
Chemische Grundlagen, Säurestärken und warum Amidosulfonsäure die beste Wahl ist
Kalkablagerungen gehören zu den häufigsten Wartungsaufgaben in der Meerwasseraquaristik. Strömungspumpen, Abschäumer, Heizer, UV‑Anlagen und Dosierleitungen arbeiten in einem Milieu, das reich an Calcium und Carbonat ist. Dadurch entstehen schnell harte Calciumcarbonat‑Schichten, die die Leistung der Geräte beeinträchtigen, den Energieverbrauch erhöhen und im schlimmsten Fall zu Ausfällen führen. Ein systematisches, materialschonendes und effizientes Entkalken ist daher unverzichtbar.
Kalk im Aquarium – warum er entsteht und warum er so hartnäckig ist
Calciumcarbonat (CaCO₃) ist eine der am weitesten verbreiteten Verbindungen im Meerwasser. Es tritt in zwei mineralischen Formen auf:
- Kalzit – härter löslich, z. B. in Muschelschalen, Seeigeln, Kalkrotalgen
- Aragonit – leichter löslich, z. B. in Korallenskeletten
Beide Formen lagern sich bevorzugt an warmen, strömungsreichen oder rauen Oberflächen ab – also genau dort, wo Pumpen und Abschäumer arbeiten. Da Calciumcarbonat in reinem Wasser praktisch unlöslich ist, lässt es sich nur durch Säuren zuverlässig entfernen.
Wie Säuren Kalk lösen – der grundlegende chemische Mechanismus
Die Auflösung von Kalk erfolgt durch Protonen (H⁺), die das Carbonat im Kalk angreifen. Die Reaktion läuft immer nach dem gleichen Schema:
CaCO3 + 2 H+→Ca2+ + CO2↑ + H2O
Das entstehende CO₂ sorgt für das typische Aufschäumen.
Die Geschwindigkeit dieser Reaktion hängt direkt davon ab, wie stark eine Säure ist und wie viele Protonen sie bereitstellt.
Säurestärke – der entscheidende Faktor für die Entkalkungsleistung
Die Stärke einer Säure wird über den pKa‑Wert beschrieben:
- Je niedriger der pKa‑Wert, desto stärker die Säure.
- Eine Differenz von 2 pKa‑Einheiten bedeutet bereits einen 100‑fachen Unterschied in der Protonenabgabe.
Damit wird klar:
Die Wahl der Säure entscheidet über Geschwindigkeit, Materialverträglichkeit und Effizienz.
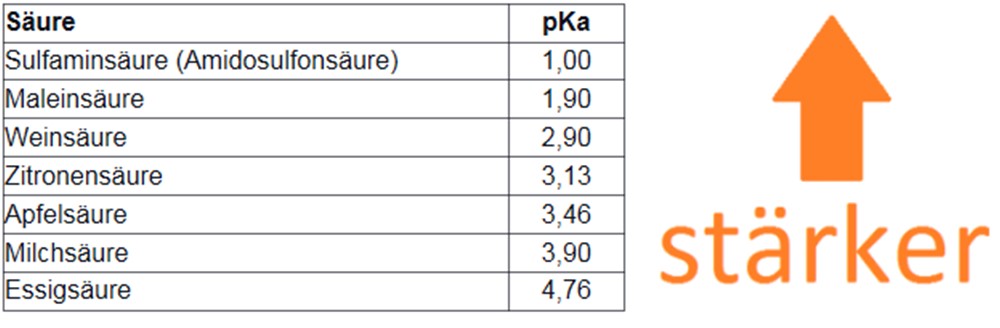
Einordnung der wichtigsten Säuren
| Säure | Stärke | Eigenschaften |
|---|---|---|
| Schwefelsäure (H₂SO₄) | stark | sehr aggressiv, materialschädigend |
| Salzsäure (HCl) | stark | löst Kalk schnell, aber korrosiv |
| Phosphorsäure (H₃PO₄) | mittel | wirksam, aber langsam |
| Amidosulfonsäure (H₂NSO₃H) | mittel | hohe Wirksamkeit, materialschonend |
| Ameisensäure (HCOOH) | mittel | aggressiv gegenüber Metallen |
| Essigsäure (CH₃COOH) | schwach | langsam, geruchsintensiv |
| Zitronensäure | schwach | bildet schwerlösliche Calciumcitrate |
Diese Übersicht zeigt:
Starke Säuren sind gefährlich und materialschädigend, schwache Säuren sind sicher, aber langsam.
Amidosulfonsäure liegt genau in der Mitte – und verbindet die Vorteile beider Welten.
Warum Amidosulfonsäure anderen Säuren überlegen ist
Amidosulfonsäure besitzt eine Kombination von Eigenschaften, die sie für die Meeresaquaristik ideal macht:
1. Hohe Säurestärke und schnelle Reaktion
Sie wirkt deutlich stärker als Zitronen‑ oder Essigsäure und entkalkt bis zu 10‑mal schneller.
Die Protonenabgabe erfolgt kontrolliert, aber effizient – ideal für Technik, die nicht beschädigt werden darf.
2. Keine Bildung störender Nebenprodukte
Zitronensäure bildet bei Wärme schwerlösliche Calciumcitrate, die sich als zusätzliche Krusten ablagern.
Amidosulfonsäure bildet keine solchen Verbindungen.
3. Materialschonend
Sie greift Kunststoffe, Keramiklager, Edelstahl und die meisten Pumpenmaterialien kaum an.
Das macht sie ideal für:
- Strömungspumpen
- Abschäumer
- Dosierpumpen
- Heizer
- UV‑Anlagen
4. Geruchsneutral
Keine stechenden Dämpfe, keine unangenehmen Gerüche – ein Vorteil gegenüber Essig oder Ameisensäure.
5. Wirkt kalt und warm
Die Reaktionsgeschwindigkeit steigt bei Wärme, ohne dass unerwünschte Nebenprodukte entstehen.
6. Sehr hohe Löslichkeit
Amidosulfonsäure löst sich bis über 200 g/L – ideal für konzentrierte, schnell wirkende Lösungen.
Vergleich der Entkalker
| Basisstoff | Stärke | Material- verträglichkeit |
Preis/ Leistung |
Geruch | Hand-
habung |
Schmutz- lösekraft |
|---|---|---|---|---|---|---|
| Amidosulfonsäure | ++ | ++ | + | ++ | ++ | — |
| Zitronensäure | – | ++ | – | ++ | ++ | — |
| Essigessenz | –– | + | – | –– | –– | — |
| Salzsäure | ++ | –– | ++ | – | –– | — |
| Ameisensäure | ++ | –– | + | –– | –– | — |
| Schwefelsäure | ++ | –– | ++ | – | –– | — |
| Phosphorsäure | ++ | + | + | – | –– | — |
Diese Tabelle zeigt klar:
Amidosulfonsäure bietet die beste Kombination aus Wirksamkeit, Materialverträglichkeit und Handhabung.
Wie viel effizienter ist Amidosulfonsäure wirklich?
- 6‑fach höhere Säurestärke
- 10‑fach höhere Geschwindigkeit
- bis zu 60‑fach höhere Wirksamkeit gegenüber typischen Zitronensäurelösungen
Praktisch bedeutet das:
Für die gleiche Entkalkungswirkung benötigt man etwa 5–10‑mal weniger Amidosulfonsäure als Zitronensäurelösung.
Diese Relation ist ein praxisnaher Erfahrungswert und erklärt, warum Amidosulfonsäure in professionellen Entkalkern Standard ist.
Anwendung in der Meeresaquaristik
Amidosulfonsäure eignet sich besonders für:
- Strömungspumpen (enge Spalte, hohe Wärme)
- Abschäumer (große Kontaktflächen)
- Dosierpumpen (feine Leitungen)
- UV‑Anlagen (Quarzglas, Dichtungen)
- Heizer
Die hohe Wirksamkeit sorgt dafür, dass:
- kurze Einwirkzeiten genügen
- selbst hartnäckige Kalzitablagerungen gelöst werden
- feinste Düsen wieder frei werden
- Geräte nach dem Spülen sofort einsatzbereit sind
Viele Aquarianer greifen zu Zitronensäure, weil sie als „natürlich“, „sanft“ oder „umweltfreundlich“ wahrgenommen wird. Diese Wahrnehmung entsteht vor allem durch den Begriff Zitrone und die Assoziation mit Lebensmitteln. Chemisch und praktisch betrachtet ist diese Einschätzung jedoch irreführend. Die vermeintlich „natürliche“ Zitronensäure ist nicht automatisch die nachhaltigere Wahl – im Gegenteil: Durch ihre geringe Wirksamkeit und die Bildung von Calciumcitraten ist sie in der Praxis oft ökologisch ungünstiger als ein effizienter, sauber reagierender Stoff wie Amidosulfonsäure.
Essigsäure hingegen ist zwar eine schwache Säure, aber materialtechnisch problematisch. Sie kann Kunststoffe aufrauen, Metallteile korrodieren und Dichtungen angreifen. Zudem hinterlässt sie organische Rückstände, die Biofilme begünstigen und die Technik schneller wieder verschmutzen lassen. Der starke Geruch erschwert die Anwendung zusätzlich, besonders in Innenräumen. Viele Anwender erhitzen Essigsäure, um die Entkalkungswirkung zu steigern. Erwärmte Essigsäure greift Materialien deutlich stärker an, da die Reaktionsgeschwindigkeit steigt und Kunststoffe sowie Metalle empfindlicher reagieren. Organische Rückstände werden stärker eingebrannt, was zusätzliche Reinigungsarbeit verursacht.
Dosierung von Amidosulfonsäure
Für die Entkalkung von Strömungspumpen, Abschäumern und anderer Meerwassertechnik hat sich eine Konzentration von etwa 10 bis 20 Gramm Amidosulfonsäure pro Liter Wasser bewährt. Diese Lösung entspricht ungefähr einer ein- bis zweiprozentigen Konzentration und löst typische Kalkablagerungen innerhalb weniger Minuten vollständig auf. Bei stärkerer Verkalkung oder hartnäckigen Kalzitkrusten kann die Menge auf 30 bis 40 Gramm pro Liter erhöht werden, wodurch die Reaktion deutlich schneller abläuft. Müssen viele Geräte hintereinander gereinigt werden , werden gelegentlich auch Lösungen mit etwa 50 Gramm pro Liter eingesetzt, die eine besonders kurze Einwirkzeit ermöglichen. Die Entkalkung ist abgeschlossen, sobald die CO₂‑Entwicklung nachlässt und keine Bläschen mehr aufsteigen. Anschließend genügt ein gründliches Spülen unter Leitungswasser, damit die Geräte sofort wieder einsatzbereit sind.
Fazit
Amidosulfonsäure ist die effektivste und zugleich materialschonendste Säure zum Entkalken von Meerwassertechnik. Sie verbindet die hohe Wirksamkeit starker Säuren mit der Sicherheit und Materialverträglichkeit schwächerer Säuren – ohne deren Nachteile. Durch ihre hohe Säurestärke, schnelle Reaktionsgeschwindigkeit und problemlose Anwendung ist sie die erste Wahl für Strömungspumpen, Abschäumer und alle kalkbelasteten Komponenten im Meerwasseraquarium.

